అనాది నుండీ మానవుడు తన చుట్టూ ఉన్న ప్రపంచాన్ని వర్గాలుగా విడగొట్టి చూడడం అలవాటు చేసుకున్నాడు. సగుణబ్రహ్మము త్రిగుణాత్మకం అన్నాడు. చాతుర్వర్ణ్యం మయాసృష్టం అన్నాడు గీతాచార్యుడు. ద్వివర్గం రసాయనం అన్నాడు బెర్జీలియస్. ఈ ఆచారాలన్నీ సంప్రదాయికంగా వస్తూన్నవే అయినా ఇలాంటి వర్గీకరణలు అంత తేలికగా లొంగేవి కావు; మినహాయింపులు ఉంటూనే ఉంటాయి! ఉదాహరణకి, రసాయన మూలకాలు దరిదాపుగా 110 ఉన్నా వాటిని స్థూలంగా లోహములు, అలోహములు అని రెండు వర్గాలుగా విభజించి అధ్యయనం చెయ్యడం ఆనవాయితీగా వస్తూన్న ఆచారం. ఈ వర్గీకరణ ఎంతవరకు సఫలం అయిందో ఇక్కడ విచారిద్దాం.
1. లోహముల లక్షణాలు
మానవుడు సాంకేతికంగా అభివృద్ధి చెందే ప్రయాణంలో లోహములు (metals) కీలకమైన పాత్ర వహించేయనడంలో సందేహం లేదు. అందుచేత చాలమందికి లోహములంటే ఏమిటో, వాటి గుణగణాలు ఏమిటో అనుభవపూర్వకంగా తెలిసే ఉంటుంది. సర్వసాధారణంగా లోహాలకి ఉండే లక్షణాలు: (1) వాటికి ఒక రకమైన మెరుపు లేదా తళుకు (lustre) ఉంటుంది; లేకపోతే మెరుగు పెట్టి మెరుపు తెప్పించవచ్చు. (2) అవి ముట్టుకుంటే చేతికి చల్లగా తగులుతాయి. (3) అవి త్వరగా వేడెక్కుతాయి లేదా, వాటి ఉష్ణ వాహకత (heat conductivity) ఎక్కువ. (4) వాటి విద్యుత్ వాహకత (electrical conductivity) కూడా ఎక్కువే! (5) ఈ వస్తువులని సుత్తితో కొడితే ఖంగుమని మోగుతాయి. (6) ఒంచితే ఒంగుతాయి, సాగదీస్తే తీగలా సాగుతాయి. ఈ లక్షణాన్ని తాంతవత (ductility) అంటారు. (7) సుత్తితో బాదితే పలచబడి గట్టిబడతాయి. ఈ లక్షణాన్ని అఘాత వర్ధనీయత ((malleability) అంటారు. (8) ఇవి సర్వసాధారణంగా బరువుగా ఉంటాయి. (9) ఇవి వేడి చేస్తే కరుగుతాయి. ఇలా ఈ జాబితాని పొడిగించుకుంటూ పోవచ్చు.
అన్ని లోహాలూ, అన్ని వేళలలోనూ ఈ లక్షణాలన్నిటిని ప్రదర్శించక పోవచ్చు. అలాగే ఈ లక్షణాలు ఉన్నంత మాత్రాన అవి లోహాలవాలని నియమం ఏమీ లేదు. ఉదాహరణకి గాజుని గోటితో మీటితే టింగుమని శబ్దం చేస్తుంది కదా; గాజు (glass) లోహం కాదని మనందరికీ చెప్పకనే తెలుసు! సీసం (lead), తగరం (tin) లోహాలయినప్పటికీ అవి టింగు మనవు, ఖంగు మనవు. పోత ఇనుము (cast iron) పెళుసుగా ఉంటుంది. అలూమినం (aluminum), మగ్నం (magnesium) తక్కువ సాంద్రత కలవి కనుక తేలికగా ఉంటాయి. గ్రాఫైట్కి (graphite) -లోహం కాకపోయినా- వాహక శక్తి ఎక్కువ అవడమే కాకుండా మెరుగు పెట్టి తళుకు తెప్పించవచ్చు. ఇలా మినహాయింపులు చెప్పుకుంటూ పోతే ఒక వస్తువు లోహమా, కాదా అని నిశ్చయించడానికి ఏయే లక్షణాలని పరిశీలించాలో నిర్ధిష్టంగా చెప్పడం కష్టం అయిపోతుంది! ఇదే విధంగా మన అనుభవ పరిధిలో ఏది లోహం, ఏది సంయోగధాతువు (alloy) అని నిర్ధారించి చెప్పడం కూడ కష్టమే!
2. మూలకాలలో రకాలు
ఉదజని (hydrogen) నుండి యురేనియం దాకా ఉన్న 92 రసాయన మూలకాలలో 68ని లోహములనిన్నీ, 19ని అలోహములు (non-metals) అనిన్నీ, పెద్దలు ఒప్పుకుంటున్నారు; మిగిలిన అయిదింటిని ఉపలోహములు (metalloids) అనేవారు కానీ వీటిని ఇటీవలి కాలంలో అర్ధవాహకాలు (semiconductors) అని పిలవడం మొదలు పెట్టేరు. ఈ 68లో కొన్ని భూమి మీద విస్తారంగా దొరికేవే, కాని కొన్ని చాలా అరుదు. పట్టిక 1ని పరిశీలించి చూస్తే మనకి బాగా పరిచయం అయిన లోహాలు నిజానికి అంత విస్తారంగా దొరికే లోహాలు కానే కాదని తెలుస్తుంది.
పట్టిక 1. భూమి మీద ఏయే మూలకాల లభ్యత ఎంతెంత శాతం ఉందో చూపే పట్టిక.
| అలూమినమ్ | 7.45 | ఆమ్లజని (oxygen) | 49.13 |
| ఇనుము (Iron) | 4.20 | సిలికాన్ | 26.00 |
| ఖటికం (Calcium) | 3.25 | ఉదజని (Hydrogen) | 1.00 |
| సోడియం | 2.40 | కర్బనం (Carbon) | 0.35 |
| పొటాసియం | 2.35 | హరితం (Chlorine | ) 0.20 |
| మగ్నం (Magnesium) | 2.35 | భాస్వరం (Phosphorous) | 0.12 |
| టైటేనియం | 0.61 | గంధకం (Sulfur) | 0.10 |
| బేరియం | 0.05 | ఫ్లోరీన్ | 0.08 |
| స్ట్రోంషియం | 0.04 | నత్రజని | 0.04 |
| క్రోమియం | 0.03 | ||
| జిర్కోనియం | 0.025 | ||
| వెనేడియం | 0.02 | ||
| నికెల్ | 0.02 | ||
| యశదం (Zinc) | 0.02 | ||
| రాగి (Copper) | 0.01 |
ఉదాహరణకి పై పట్టికలో చిట్టచివర ఉన్న – అనగా, భూమి పై అంత పుష్కలంగా దొరికే మూలకం కాకపోయినప్పటికీ – రాగి ఉనికి మానవుడికి 5,000 సంవత్సరాలబట్టీ తెలుసు. ఆమాటకొస్తే మానవుడికి చిరకాలం నుండీ తెలిసున్న వెండి, బంగారం, సీసం ఈ పట్టికలో లేనే లేవు! పై పట్టికలో, లభ్యతలో, రెండవ స్థానంలో ఉన్న ఇనుము వాడకం మిగిలిన లోహాలన్నిటి సమష్టి వాడకం కంటె ఎక్కువ. ఇనుము తరువాత ఎక్కువ వాడకంలో ఉన్నవాటిల్లో పేర్కొనదగ్గవి మగ్నం, రాగి, అలూమినం, యశదము (zinc).
‘రాచ లోహములు’ అనదగ్గ బంగారం, ప్లాటినం, రాచరికం కాసింత లోపించిన వెండి, రాగి – ఈ నాలుగూ భూమి పైపొరలలో లోహం రూపంలో అప్పుడప్పుడు దొరుకుతాయి. మిగిలిన లోహాలు అన్నీ రసాయన సంయోగాలుగా లభ్యం అవుతాయి; ఇవి ఆమ్లజనితో సంయోగం పొందిన ఆమ్లజనిదములు (oxides) కావచ్చు, గంధకంతో సంయోగం చెందిన గంథకిదములు (sulfides), గంథకితములు (sulfates) కావచ్చు, కర్బనంతో సంయోగం చెందిన కర్బనితములు (carbonates) కావచ్చు, లేదా సంక్లిష్ట సంయోజితాలు (complex compounds) కావచ్చు. గనులలో దొరికే సంయోజితాలని ఖనిజములు (ores) అంటారు. ఈ ఖనిజాలని క్షయీకరించి (reduce చేసి, అనగా ఆమ్లజనిని బయటకి లాగి) వీటిలో దాగున్న లోహాలని వెలికి తీస్తారు. ఇలా వెలికి తీసిన ఉత్తర క్షణం నుండీ ఆ లోహాలు తమ పూర్వ స్థితిలోకి జారుకుందుకి అలా ప్రయత్నిస్తూనే ఉంటాయి. ఇనుము తుప్పు పట్టడం (rusting), రాగి కిలుం పట్టడం (verdigris) ఈ ప్రక్రియకి ఒక రకం ఉదాహరణలు. ఇక్కడ జరిగే ప్రక్రియని ఆక్సీకరణం (oxidation) అంటారు. వెండి ఆక్సీకరణం చెందదు కానీ అది నల్లబడడానికి (tarnishing) కారణం కల్మషపు గాలిలో ఉన్న ఉదజని గంధకిదముతో (hydrogen sulfide) కలిసి రజత గంధకిదముగా (silver sulfide) మారడం.
3. పూర్వకాలంలో
రాతియుగంలో సహజసిద్ధంగా లభించే లోహపు కణికలు మానవుడి కంటికి కనబడినప్పుడు రాళ్ళకీ, ఆ కణికలకి మధ్య తేడా స్పుటంగా ఉండడం గమనించి వాటిని పదిలంగా భద్రపరచి ఉంటాడు. ఆకుపచ్చగా ఉండే తామ్ర కర్బనితం (copper carbonate) రాళ్ళనీ, నల్లగా ఉండే అంజన గంధకిదము (antimony sulphide) లేదా సుర్మా రాళ్ళనీ గుండ చేసి ఈజిప్టులోని పురాతన (సా. శ. పూ. 3500) రాజవంశీయులు సౌందర్య సామగ్రులుగా ఉపయోగించినట్లు దాఖలాలు ఉన్నాయి. వీటిని బొగ్గుల కొలిమిలో వేడి చేస్తే తేలికగా క్షయీకరణ పొంది, వాటిలోని లోహం బయటకి వచ్చేస్తుంది కనుక మూడొంతులు ప్రాచీనులకి రాగి, అంజనం లేదా సుర్మా (antimony) పరిచయమైన లోహాలే అయి ఉండవచ్చు. రోమను సామ్రాజ్యం వెల్లివిరిసేనాటికి (సా. శ. పూ. 200) ఇనుము, రాగి, సీసం, తగరం, పాదరసం, వెండి, బంగారం విస్తారంగా వాడుకలోకి వచ్చేసేయి కనుకనే ‘లోహం’ అనగానే ఈ ఏడు మూలకాలు ఠకీమని స్పురణకి వస్తాయి. ఇవన్నీ ఎక్కువ సాంద్రత కలిగినవి, మెరుగు పెడితే మెరిసేవి, తాకగానే చేతికి చల్లగా తగిలేవీను. ఒక్క పాదరసాన్ని మినహాయిస్తే ఇవన్నీ సుతిమెత్తనివి (malleable), సుత్తితో బాదితే గట్టిబడేవి, వేడి చేస్తే మెత్తబడేవీ. వీటిని వేడి చేసి కరిగించవచ్చు, ఒకదానితో మరొకదానిని కలిపి, కరిగించి సంయోగధాతువులుగా (alloys) చెయ్యవచ్చు.
మన పూర్వులు సంయోగధాతువులతో విశేషంగా పని చేసేరు కాని లోహములకీ సంయోగధాతువులకీ మధ్య ఉన్న తేడాలు వారికి పరిపూర్ణ అవగాహనలోకి వచ్చిన దాఖలాలు మాత్రం లేవు; ఏదో గుడ్డి గుర్రపు తాపులా వారికి కొన్ని సంయోగధాతువులు తారసపడి ఉండొచ్చు. ఇలాంటి సందర్భాలలో అప్పటివరకు ఎరికలో లేని మూలక లోహాలు (metal elements) వారు చూసినా అవి లోహాలని వారి గ్రహింపుకి వచ్చి ఉండకపోవచ్చు. ఒక గనిలో దొరికిన ఖనిజపు రాయిని ఒక విధంగా ‘ప్రక్షాళిస్తే’ వచ్చిన లోహం మరొక చోట దొరికిన ఖనిజం మీద అదే పద్ధతి ప్రయోగిస్తే పని చేసేది కాదు. ఉదాహరణకి రోమనులకి మూడు రకాల ‘సీసము’ల గురించి తెలుసు: సాధారణ సీసం (Plumbum nigrum), తగరం (Plumbum candidum అనగా, బ్రిటన్ నుండి వచ్చిన సీసం), బిస్మత్ (Plumbum cinereum). అలాగే వారు రాగిని సైప్రస్ కంచు (aes cyprium అనగా సైప్రస్లో దొరికే కంచు) అనేవారు. పదిహేను వందల సంవత్సరాల తరువాత కూడ, జెర్మనీలోని రాగి కమ్మటాలలో (copper smelters) కోబాల్ట్కీ నికెల్కీ మధ్య తేడా తెలియక తికమకలు పడ్డారనడాని వాటి పేర్లే సాక్ష్యం. (జెర్మన్ భాషలో నికెల్ అన్నా కోబాల్ట్ అన్నా భూతం అనీ డాకినీ అని అర్థం!)
4. 18వ శతాబ్దంలో
పద్దెనిమిదవ శతాబ్దం వచ్చేసరికి మన అవగాహన బాగా పెరిగింది; ఖనిజాలు చాలమట్టుకి లోహాలతో కలిసిన మిశ్రమ పదార్థాలు (compounds) అన్న గ్రహింపు రాగానే వాటి నుండి లోహాలని వెలికి తియ్యడం ఎలాగో కష్టపడి తెలుసుకున్నారు. అయినప్పటికీ ఏది లోహం, ఏది కాదు అనే మీమాంస వచ్చినప్పుడల్లా పూర్వపు తొమ్మిది అంశాల కొలబద్దని వాడడంలో ఇబ్బంది పడేవారు. ఉదాహరణకి సా. శ. 1743 లో యశదము (zinc) ‘మెరుపులోనూ, విశిష్ట గురుత్వం (specific gravity) లోనూ, వేడి చేసినప్పుడు కరగడం లోనూ లోహంలా అనిపించినా, మంటలో వేసినప్పుడు భగ్గుమని మండే లక్షణాన్ని బట్టి లోహం కాదేమో’ అని తటపటాయించేవారు. రంగులోనూ, బరువులోనూ, ఆకారంలోనూ లోహంలా అనిపించినా పెళుసుతనం (not malleable) వల్ల కోబాల్ట్ని అర్ధలోహం (half metal) అనేవారు.
5. 19వ శతాబ్దంలో
పందొమ్మిదవ శతాబ్దం ఆరంభదశ వరకు లోహాలని ఖనిజాలనుండి వేరు చెయ్యడానికి బొగ్గుతో కలిపి కొలిమిలో పెట్టి వేడి చేసి (smelting) క్షయీకరించడం (reduction) ఆచరించదగ్గ పద్ధతిగా ఉండేది. కానీ డేవీ (Devy), ఫేరడే (Faraday), చేసిన ప్రయోగాల ఫలితంగా క్షయీకరణకి బదులు విద్యుత్తుని వాడడం తెలియగానే సోడియం (sodium), పొటాసియం (potassium) లను వాటి ఖనిజాల నుండి వేరు చెయ్యడం తెలిసింది. మిగిలిన లోహాలతో పోల్చితే ఈ రెండు లోహాలు ప్రత్యేకమైనవి. ఈ రెండూ జున్నులా మెత్తగా ఉండి కత్తితో కొయ్యడానికి వీలుగా ఉండడమే కాకుండా, ఇవి అత్యంత చురుకుదనం గలవి, నీటి కంటె తేలికైనవీ అయిన లోహాలు! ఈ చురుకుదనం అనే లక్షణాన్ని ఉపయోగించుకుని – అనగా ‘వాడుకుని’ – క్షయీకరణకి లొంగని ఖనిజాల నుండి ఖటికం (calcium), మగ్నం (magnesium), అలూమినం లని విడదీయడం జరిగింది. తరువాత ఎక్కువ వేడి పుట్టించే కొలిమిలని నిర్మించడం అర్థం అయిన పిమ్మట ఇంకా మొండి ఘటాలైన వెనేడియం, నియోబియం, టేంటలం, వగైరా లోహాలని వాటి వాటి ఖనిజాల నుండి, వ్యయప్రయాసలతో, ఎట్టకేలకు వేరు చేసేరు.
6. రసాయన దృక్పథంలో
పందొమ్మిదవ శతాబ్దం వరకు మూలకం (element) అనేదానిని కేవలం రసాయన దృక్పథం తోటే చూసేవారు. కనుక మూలకాల వర్గీకరణ సమయంలో ఏది లోహం? ఏది కాదు? అన్న ప్రశ్నలు రసాయన దృక్పథంతోనే ముందుకు వచ్చేవి. ఉదాహరణకి రసాయనుల దృష్టిలో లోహానికి ఉండవలసిన లక్షణాలు మూడు: (1) లోహము ఆమ్లజనితో సంయోగము చెంది భస్మం అయినప్పుడు ఆ భస్మాన్ని (oxide) ఆమ్లములలో కరిగిస్తే లవణాలు (salts) పుడతాయి. (అలోహాల భస్మాలే ఆమ్లాలు!) (2) లోహాల వల్ల పుట్టిన లవణాలు ద్రావణంలో ఉన్నప్పుడు విద్యుత్-ధన ఆవేశం (electro-positive charge) కలిగిన అయానులు పుడతాయి కనుక అవి విద్యుత్ ఘటంలో (electrolytic cell) ఋణ ధ్రువం దగ్గరకి చేరుతాయి. (అలోహాలు విద్యుత్-ఋణ ఆవేశం చూపుతాయి!) (3) లోహాలతో తయారయిన హరిదములు (chlorides) నీటిలో స్థిరత్వం కలిగి ఉంటాయి. (అలోహాలతో తయారయిన హరిదములు నీరు తగలగానే శిధిలం (decompose) అయిపోతాయి – అప్పుడప్పుడు తీవ్రముగా (violent).
ఇలా రసాయనుల కోణంలో చూస్తే లోహాలు అనే కిరీటం ధరించడానికి అర్హత ఉన్న వాటిల్లో ప్రథమస్థానం క్షారలోహాలైన సోడియం, పొటాసియంలకు ఇవ్వాలి! ఆధునికుల దృష్టిలో ఈ మాటంటే నగుబాటు! నిజమే, ఈ రెండూ తేలికగా కరుగుతాయి (సోడియం 970C దగ్గరా, పొటాసియం 630C దగ్గరా ‘కరుగు’ అనగా melt అవుతాయి) కాని ఈ రెండు ఇతర లోహాలతో ఎక్కువ సంయోగం చెందవు. ఈ రెండూ కత్తితో కొయ్యగలిగే అంత మెత్తగా ఉంటాయి, ఒంగుతాయి. క్షార లోహాలయిన లిథియం, సోడియం, పొటాసియంల సాంద్రత చాల తక్కువ; ఇవి నీటి మీద తేలుతాయి! లిథియం బెండు కంటె తేలిక! (విశిష్ట గురుత్వం = 0.59). ఇంత మెత్తగా ఉన్న వీటిని లోహాలనడానికి మనస్సు ఒప్పుకోదు.
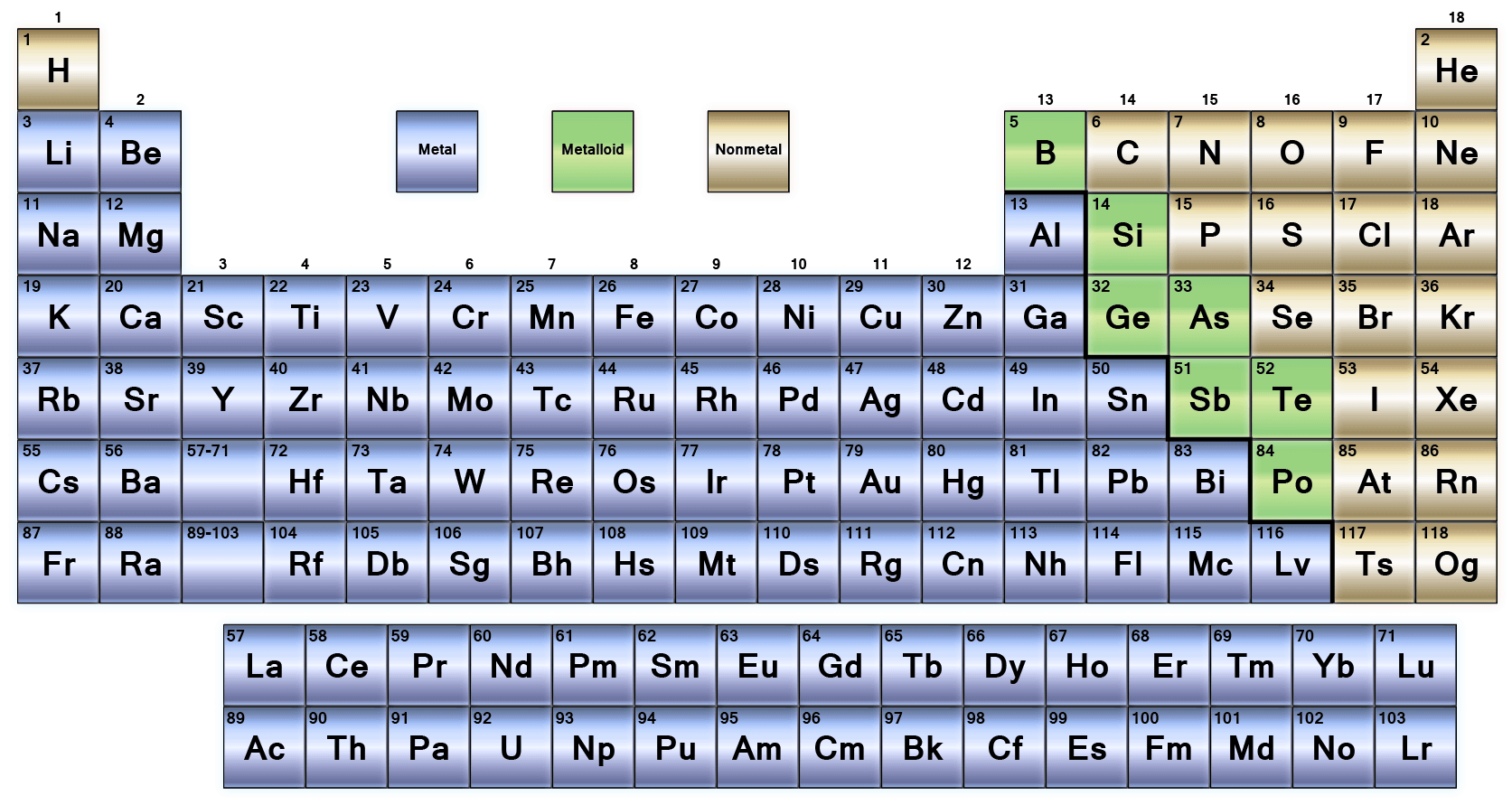
బొమ్మ 1. ఆవర్తన పట్టిక (గూగుల్ సౌజన్యంతో).
7. ఆవర్తన పట్టిక చెప్పిన తీరు
ఆవర్తన పట్టికలో (The Periodic Table) లోహాలని, అలోహాలని విడదీస్తూ బొద్దుగా, మెట్ల రూపంలో, ఒక గీత గీస్తూ ఉంటారు. (బొమ్మ 1లో లోహాలని నీలంగానూ, అలోహాలని బంగారురంగుగానూ చూపించడం జరిగింది.) ఈ ‘గీతకి’ దిగువన, ఎడం పక్కన ఉన్నవి లోహాలు; ఎగువన, కుడి పక్క ఉన్నవి అలోహాలు అని రివాజుగా తీర్మానిస్తూ ఉంటారు. ఈ ఆచారానికి విరుద్ధంగా కొన్ని ఉదాహరణలని చూపవచ్చు. మచ్చుకి భౌతిక లక్షణాలని బట్టి నీలపు గది 4లో ఉన్న బెరిలియం (Be), నీలపు గది 13లో ఉన్న అలూమినం (Al) నిస్సందేహంగా లోహాలే కాని వాటి భస్మాలు ఒకొక్కప్పుడు ఆమ్ల లక్షణాలని, మరొకప్పుడు క్షార లక్షణాలని చూపుడమే కాకుండా, వాటి హరిదములు నీరు తగలగానే కోపగించుకుని ‘ఖస్సు’ మంటాయి. మరొక ఉదాహరణగా 7వ గదిలో ఉన్న నత్రజని (nitrogen, N), దాని దిగువన 15వ గదిలో ఉన్న భాస్వరము (phosphorous, P) సంగతి చూద్దాం. ఈ రెండూ ఒకే నిలువు వరసలో (కుటుంబంలో) ఒకదాని కింద ఒకటి ఉండి రెండూ అలోహాలు గానే ప్రవర్తిస్తాయి. ఆకుపచ్చ 33వ గదిలో ఉన్న ఆర్సెనిక్ (As) లోహంలా అనిపించినా అలోహంలా ప్రవర్తిస్తుంది; దానికి రెండు వరసల దిగువన 83వ నీలం గదిలో ఉన్న బిస్మత్ (Bi) మూడొంతుల ముప్పాతిక లోహం లాగనే ఉన్నా పెళుసుగా ఉంటుంది. పైపెచ్చు దాని హరిదం (chloride) నీటి పొడలో నిశ్చలంగా బతకలేదు. సరిహద్దులో ఉన్న అలోహాలన్నీ – అనగా, 5వ గదిలో ఉన్న బోరాన్ (B), 14వ గదిలో ఉన్న సిలికాన్ (Si), 32వ గదిలో ఉన్న జెర్మేనియం (Ge), 33వ గదిలో ఉన్న ఆర్సెనిక్ (As), 52వ గదిలో ఉన్న టెలూరియం (Te), చిట్టచివరికి 6వ గదిలో గ్రాఫైట్ రూపంలో ఉన్న కర్బనం (C) – చూడడానికి లోహాలలా అనిపిస్తాయి.
రసాయనులు ఆవర్తన పట్టికతో ఇలా కుస్తీలు పడుతూ ఉంటే తరవాయి కార్యక్రమాన్ని నడిపే బాధ్యత భౌతిక శాస్త్రవేత్తల భుజాల మీద పడిందనవచ్చు. పందొమ్మిదవ శతాబ్దపు రసాయన శాస్త్రవేత్తలకి అణువు (atom) అనేది మూలకము యొక్క అవిచ్ఛినమైన సూక్ష్మ రూపం. వారి దృష్టిలో ఏ మూలకపు అణువుకైనా ఒక నిర్దిష్టమైన గరిమ (mass) ఉంటుంది, ఒక నిర్దిష్టమైన బాహుబలం (valency) ఉంటుంది. (బాహుబలం అంటే ఒక మూలకం మరొక మూలకంతో రసాయన సంయోగము చెందగలిగే శక్తి.)
8. 20వ శతాబ్దంలో
ఇరవైయవ శతాబ్దం వచ్చేసరికి గుళిక వాదం (quantum theory) తలెత్తడంతో అణువుల యెడల మన అవగాహన బాగా పెరిగింది. అణువు (atom) అవిచ్ఛిన్నం కాదనిన్నీ, దాని గర్భంలో నూట్రానులు, ప్రోటానులు అనే పరమాణువులు (sub-atomic particles) ఉంటాయనిన్నీ, ఈ గర్భం చుట్టూ ఋణావేశం ఉన్న ఎలక్ట్రానులు ఉంటాయనిన్నీ తెలిసింది. ఆవర్తన పట్టికలో కుడి చివర నిలువు వరసలో (కుటుంబం) కనిపించే అచేతన (inert) వాయువులైన రవిజని (helium), నియాన్… వగైరాల కర్పరాలు (shells) అన్నీ పూర్తిగా ఎలక్ట్రానులతో నిండిపోయి ఉంటాయి కనుక వాటికి స్థిరత్వం (stability) ఎక్కువ (అనగా, చైతన్యం తక్కువ). ఈ అంశం దృష్ట్యా ఒక మూలకం యొక్క రసాయన లక్షణాలు కేంద్రకం (nucleus) చుట్టూ ఉండే ఎలక్ట్రానుల స్థిరత్వం మీద ఆధారపడి ఉంటాయని తీర్మానించవచ్చు; స్థిరత్వం తక్కువ ఉంటే చురుకుదనం ఎక్కువగా ఉంటుంది. క్షార లోహాలు (ఒకటవ కుటుంబంలో ఉన్న లిథియం, సోడియం, పొటాసియం, వగైరాలు) తమ బాహ్య కర్పరాలలో ఉన్న ఏకైక ఎలక్ట్రానుని వదలుకోడానికి సిద్ధపడతాయి కనుక అవి చాలా చురుకైన మూలకాలు అయేయి. అదే విధంగా అచేతన వాయుకుటుంబానికి ఎడం పక్కన 7వ కుటుంబంలో ఉన్న ఫ్లోరీను, క్లోరీను, వగైరాల బాహ్య కోష్టికలలో స్థిరత్వానికి కావలసిన సంఖ్య కంటె ఒక ఎలక్ట్రాను తక్కువ కావడంతో ఆ ఒక్క ఎలక్ట్రానుని సంపాదించి స్థిరత్వం పొందడానికి సదా ఆరాటపడుతూ ఉంటాయి కనుక అవి కూడా చలాకీ మూలకాలే. కనుక ఒక క్లోరీన్ (Cl) అణువు సునాయాసంగా ఒక సోడియం (Na) అణువు ఇచ్చే ఒక ఎలక్ట్రానుని స్వీకరించి స్థిరత్వం ఉన్న సోడియం క్లోరైడ్ (NaCl) అనే సంయోగ పదార్థాన్ని ఇస్తుంది. ఇలా ఎలక్ట్రాను బదిలీ అవడం వల్ల ఇంతవరకు తటస్థంగా (neutral) ఉన్న అణువులు రెండూ ఆవేశం పొందిన Cl- అయాను గాను, Na+ అయాను గాను మారతాయి. ఇలా పరస్పరం వ్యతిరేక ఆవేశాలు ఉండడం వల్ల ఈ రెండు అయానులు ఒకదానిని మరొకటి బలంగా ఆకర్షించుకుంటాయి. అందుకనే NaClకి స్థిరత్వం ఎక్కువ. ఈ రకం బంధాన్ని ‘అయానిక’ బంధం అంటారు.
ఇలా రసాయనులు చేసిన కృషి వల్ల మనకి తెలిసినది ఏమిటంటే ఆవర్తన పట్టికలో ఎడం పక్కగా ఉన్న నిలువు వరుసలలోనూ (కుటుంబాలలోనూ), దిగువగా ఉన్న అడ్డు వరుసలలోనూ (ఆవర్తులలోనూ) ఉన్న మూలకాలు లోహాలు అయి ఉంటాయి.
9. భౌతిక శాస్త్రపు కోణంలో
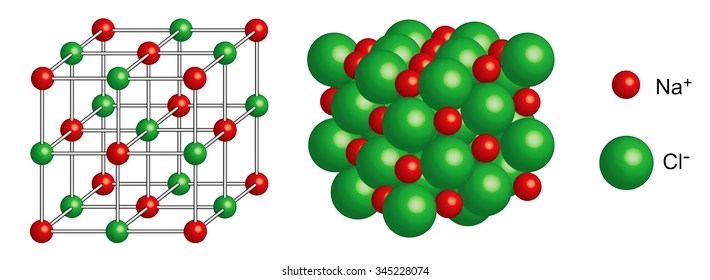
బొమ్మ 2. సోడియం క్లోరైడ్ (ఉప్పు) స్పటికంలో ఉండే సోడియం అయానులు (ఎర్ర బంతులు), క్లోరీన్ అయానులు (ఆకుపచ్చ బంతులు) ఘనచతురస్రం ఆకారంలో ఎలా అమరి ఉంటాయో చూపే పటం (గూగుల్ సౌజన్యంతో).
ఇప్పుడు భౌతిక శాస్త్రపు కోణంలో చూద్దాం. ఘన రూపంలో ఉన్న సోడియమ్ క్లోరైడ్ని (ఉప్పు) నిశితంగా పరిశీలించి చూస్తే అందులో ఉన్న ధన సోడియం అయానులు (Na+), ఋణ క్లోరీన్ అయానులు (Cl-) ఏకాంతర (alternate) స్థానాలలో బారులు తీర్చిన బంతుల మాదిరి మూడు దిశలలోనూ వ్యాపించి ఉంటాయి (బొమ్మ 2 చూడండి). ఈ రకపు అమరికకి స్థిరత్వం ఎక్కువ, దృఢత్వం (అనగా, వంగకుండా ఉండే, బీటలు పడకుండా ఉండే కఠినత్వం లేదా rigidity) ఎక్కువ. ఎందుకంటే, వంగాలన్నా, బీటలు పడి విరగాలన్నా పరస్పరం వ్యతిరేకంగా ఉన్న ధన, ఋణ విద్యుత్ అయానుల మధ్య ఉండే దృఢమైన అయానిక్ బంధం తెగ్గొట్టాలి.
మరొక ఉదాహరణగా వజ్రంలో కర్బనం (carbon) అణువుల అమరికని పరిశీలించి చూద్దాం. కర్బనం అణువు యొక్క బాహ్య కర్పరంలో (outer shell) నాలుగు ఎలక్ట్రానులే ఉంటాయి కాని ఈ కర్పరంలో ఎనిమిది ఎలక్ట్రానులు పట్టడానికి సరిపడా చోటు ఉంది. కనుక ప్రతి కర్బనం అణువు తన పొరుగున ఉన్న కర్బనం అణువుతో నాలుగు ఎలక్ట్రానులని ఉమ్మడిగా పంచుకోగలదు. ఇప్పుడు ఒకొక్క కర్బనం అణువు పొరుగున నాలుగేసి ఇతర కర్బనం అణువులు ఉండేటట్లు అమర్చితే, ప్రతి కర్బనం అణువుకి తనవి నాలుగు, తన పొరుగున ఉన్న నాలుగు కర్బనం అణువుల నుండి ఒకొక్కటి చొప్పున మొత్తం నాలుగు తీసుకుని తన కర్పరాన్ని ఎనిమిది ఎలక్ట్రానులతో నింపుకుని స్థిరత్వం, దృఢత్వం పొందగలదు. ఈ రకం అమరిక కావాలంటే కర్బనం అణువులని మూడు దిశలలో వ్యాపించి ఉన్న చతుష్ఫలకం (tetrahedron) ఆకారంలో అమర్చాలి. వజ్రంలో ఉన్న కర్బనం ఈ అమరికలోనే ఉంటుంది కనుక అది అంత దృఢంగా (hard) ఉంటుంది. (పెళుసుగా కూడా ఉంటుంది కాని అది వేరే విషయం!) ఈ రకం బంధాన్ని నిరూపక బంధం (co-ordinate bond) అంటారు.
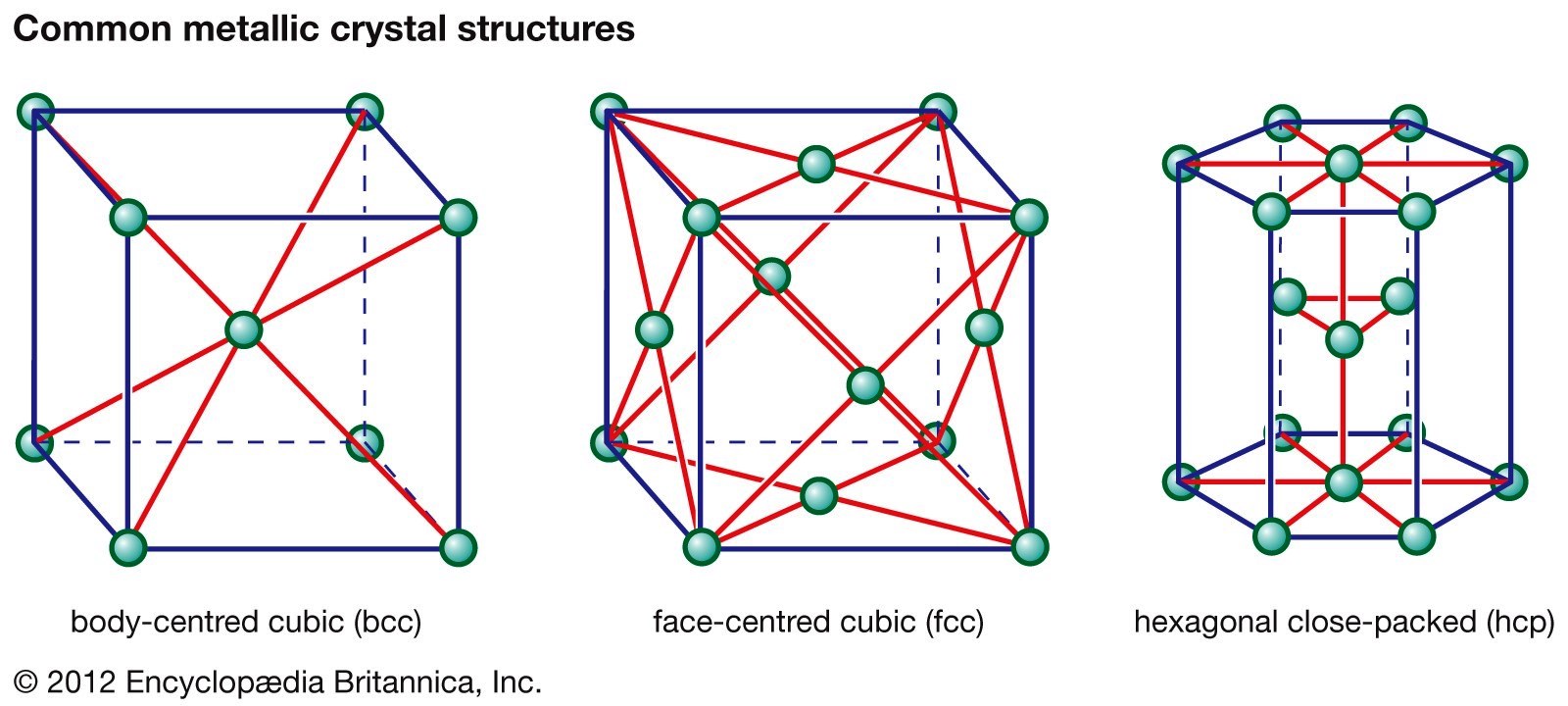
బొమ్మ 3. దరిదాపుగా లోహములన్నిటిలోనూ అణువులు (లేదా అయానులు) పైన చూపిన మూడు విన్యాసాలలో ఏదో ఒక విన్యాసాన్ని ప్రదర్శిస్తాయి. Body-centered cubic అంటే ఘనచతురస్రం పొట్టలో ఒక శాల్తీ, ప్రతీ మూల లోను ఒక శాల్తీ ఉన్న విన్యాసం. Face-centered cubic అంటే ఘనచతురస్రం యొక్క ప్రతి ముఖం మీద ఒక శాల్తీ, ప్రతీ మూల లోను ఒక శాల్తీ ఉన్న విన్యాసం. ఏయే లోహాలు ఏయే విన్యాసాలలో ఉంటాయో పట్టిక 2లో చూడవచ్చు (గూగుల్ సౌజన్యంతో).
పైన ఉదహరించిన ఉప్పు, వజ్రం లోహాలు కావు. ఇప్పుడు లోహపు సోడియంలో (metallic sodium) అణువుల అమరిక ఎలా ఉంటుందో చూద్దాం. సోడియం అణువులు తమ బాహ్య కర్పరంలో ఒంటరిగా ఉన్న ఎలక్ట్రానుని వదలుకోగా మిగిలిన అయానులు, ఒకదానికి మరొకటి సమాన దూరంలో ఉండేటట్లు, మూడు దిశలలోనూ బారులు తీర్చిన ఇటికలలా అమరిపోతాయి. ఒంటరి ఎలక్ట్రానులన్నీ జారుడుగా ఉన్న ఉమ్మడి బెందడిలా సోడియం అణువుల మధ్య విశృంఖలంగా తిరుగాడుతూ విద్యుత్పరంగా తటస్థతని ప్రదర్శిస్తాయి. ఈ రకం అమరికని body-centered cubic అంటారు (బొమ్మ 3లో ఎడం పక్క బొమ్మ చూడండి). ఈ అమరికలో ఒక ఘనచతురస్రం లేదా ఘనానికి (cube) ఉన్న ఎనిమిది మూలలోనూ ఒకొక్క అణువు, ఘనం మధ్య ఒక అణువు ఉంటాయి. రాగిలో ఉండే అణువులని ఇంతకంటే కుదిమట్టంగా (compact) అమర్చవచ్చు. ఈ రకం అమరికని face-centered cubic అంటారు (బొమ్మ 3లో మధ్యనున్న బొమ్మ చూడండి). ఈ అమరికలో ఒక ఘనానికి ఉన్న ఎనిమిది మూలలోనూ ఒక అణువు, ఆరు ముఖాల మధ్య ఒకొక్క అణువు ఉంటాయి. యశదం (zinc) లోని అణువులు hexagonal close pack అనే అమరికలో ఉంటాయి (బొమ్మ 3లో కుడి చివర బొమ్మ చూడండి).
పైన పేర్కొన్న మూడు లోహపు స్పటికాకారాలు (metallic crystal structures) – అనగా body-centered, face-centered, hexagonal close packed – చాల ప్రత్యేకమైనవి. వీటిని సోడియం క్లోరైడ్, కర్బనాల స్పటికాకారాలతో పోల్చి చూద్దాం. మొట్టమొదటగా వీటిలోని బాలపు ఎలక్ట్రానులు (valence electrons) తమ తమ ‘మాతృ’ అణువుతో నిమిత్తం లేకుండా, విశృంఖలంగా, ఒక ‘ఉమ్మడి ఎలక్ట్రాన్ సరస్సు’లో (electron lake) తిరుగుతూ ఉంటాయి. వివిక్తంగా (isolated) ఉన్న స్పటికంలో ఈ తిరుగుడు యాదృచ్చికంగా ఉంటుంది – అనగా, ఈ తిరుగుడుకి ఒక నిర్దిష్టమైన దిశ అంటూ ఉండదు. కాని ఈ స్పటికాన్ని ఒక విద్యుత్ క్షేత్రంలో (electric field) పెడితే, యాదృచ్చికంగా ఉన్న కదలిక ఒక ప్రవాహంలా మారుతుంది. అందుకనే ‘లోహాలు విద్యుత్ వాహకత్వాన్ని చూపుతాయి’ అంటాము. ఈ విద్యుత్ వాహకత్వం కారణంగానే లోహాలు ఉష్ణవాహకత్వాన్ని కూడా సంతరించుకుంటాయి. (ఎందుకంటే, ఎలక్ట్రానులు ‘ఉష్ణ కంపనాలని’ కూడా సమర్ధతతో మోసుకునిపోగలవు!) ఈ విద్యుత్ వాహకత్వం వల్లనే మెరుగు పెట్టిన లోహాలు కాంతిని అద్దంలా పరావర్తిస్తాయి. (ఎందుకంటే, పెద్ద లోహపు రేకు పొడుగాటి రేడియో తరంగాలని సమర్ధతతో పరావర్తించినట్లే, బుల్లి రేకు పొట్టిగా ఉండే కాంతి తరంగాలని సమర్ధతతో పరావర్తనం చేస్తుంది!) అందుకనే మెరుగు పెట్టిన వెండి కాంతిని పరావర్తించడమే కాకుండా ఉత్తమోత్తమమైన ఉష్ణవాహకత్వాన్ని కూడా ప్రదర్శించడంలో ఆశ్చర్యపడవలసిన అవసరం లేదు.
ఇదే ధోరణిలో ఆలోచించి లోహాలు ప్రదర్శించే మరొక లక్షణాన్ని కూడా సమర్ధించవచ్చు. గుండ్రంగా ఉన్న గోళీలని రకరకాల విన్యాసాలలో అమర్చవలసి వచ్చినప్పుడు కొన్ని విన్యాసాలలో ఎక్కువ దట్టంగా గోళీలని కుక్కవచ్చు. అలానే ఒక స్పటికంలో అణువులని అనేక విన్యాసాలలో అమర్చవచ్చు కానీ కొన్ని ప్రత్యేకమైన విన్యాసాలలో ఎక్కువ అణువులని దట్టించి కుక్కవచ్చు. ఈ కోణంలో చూసినప్పుడు సర్వసాధారణంగా లోహపు అణువులు ఎక్కువ దట్టంగా ఉన్న విన్యాసాలలో అమురుతాయి. అందుకనే లోహాల సాంద్రత అలోహాల సాంద్రత కంటె ఎక్కువ. (లోహాల అధిక సాంద్రతకి సిసలైన అసలు కారణం కర్బనం, గంధకం వంటి అలోహాలతో పోల్చి చూస్తే రాగి, సీసం వంటి లోహాల అణు భారాలు ఎక్కువగా ఉండడమే!) ఈ లక్షణాలు ఉన్న స్పటికాల నిర్మాణ శిల్పం మరొక విధంగా కూడా లోహాల గుణగణాలని ప్రభావితం చేస్తుంది. ఇక్కడ జరిగే ప్రక్రియ సంక్లిష్టమైనది కనుక కాసింత తేలికగా చెప్పడానికి ప్రయత్నిస్తాను. స్పటికాల మీద ఒత్తిడి పెట్టినప్పుడు లోహాలలోని ‘పొరలు’ ఒకదాని మీద మరొకటి జారితే ఆ లోహాన్ని రేకులుగా సాగగొట్టవచ్చు, తీగలుగా లాగవచ్చు. ఈ పనిని face-centered cubic structure ఉన్న లోహాలతో చెయ్యడం తేలిక. ఈ లక్షణాలు (అనగా, malleability, ductility) పుష్కలంగా ఉన్న రాగి, వెండి, బంగారం face-centered cubic structureనే ప్రదర్శించడం గమనార్హం. ఇనుము body-centered cubic structureలో ఉంటుంది కనుక ఈ జారుడు లక్షణం కాసింత తక్కువ. యశదం, మగ్నం hexagonal close-packed విన్యాసంలో ఉన్నాయి కనుక వాటికి ఈ జారుడు లక్షణం ఒకే నిరూపక దిశలో (coordinate direction) ఉంటుంది. ఏయే లోహాలు ఏయే విన్యాసాలలో అమరి ఉంటాయో పట్టిక 2లో పొందుపరచేను.
పట్టిక 2. లోహాలలో కనిపించే మూడు ముఖ్యమైన స్పటిక విన్యాసాలు.
| అలూమినం (Al) | బేరియం (Ba) | బెరిలియం (Be) |
| కేల్సియం (Ca) | నియోబియం (Nb) | కేడ్మియం (Cd) |
| కాపర్ (Cu) | క్రోమియం (Cr) | కోబాల్ట్ (Co) |
| గోల్డ్ (Au) | ఐరన్ (Fe) | హేఫ్నియం (Hf) |
| ఇండియం (In) | లిథియం (Li) | లేంథనం (La) |
| లెడ్ (Pb) | మోలిబ్డినం (Mo) | మెగ్నీసియం (Mg) |
| నికెల్ (Ni) | పొటాసియం (K) | ఓస్మియం (Os) |
| పెలేడియం (Pd) | రుబీడియం (Rb) | రీనియం (Re) |
| ప్లాటినం (Pt) | సోడియం (Na) | రుథీనియం (Ru) |
| రోడియం (Rh) | టేంటలం (Ta) | థేలియం (Tl) |
| స్కేండియం (Sc) | టంగస్టన్ (W) | టైటేనియం (Ti) |
| సిల్వర్ (Ag) | వెనేడియం (V) | యిట్రియం (Y) |
| స్ట్రోంషియం (Sr) | జర్కోనియం (Zr) | |
| థోరియం (Th) | జింక్ (Zn) |
10. ముక్తాయింపు
ఆశ్చర్యం ఏమిటంటే చాలమట్టుకి లోహాలు ఈ మూడు విన్యాసాలలోనూ దరిదాపుగా సమానంగా సర్దుకున్నాయి! ఈ పట్టికలో చోటు చేసుకోకుండా మిగిలిపోయిన లోహాలు లేకపోలేదు. ఉదాహరణకి ఏంటిమొనీ, బిస్మత్ ఈ పట్టికలో లేవు. దానికి కారణం వాటి విన్యాసాలు లోహపు విన్యాసాలలా ఉండక అలోహమైన ఆర్శెనిక్ని పోలి ఉండడమే. ఆమాటకొస్తే ఈ రెండూ అలోహాల వలె పెళుసుగా ఉంటాయి, వాటి విద్యుత్ వాహకత్వం కూడా తక్కువే. ఈ పట్టిక లోకి ఎక్కకుండా తప్పించుకున్న మరొక లోహం తగరం. దీని విన్యాసం గోడ మీది పిల్లిలా ఉష్ణోగ్రతని బట్టి మారుతూ ఉంటుంది; ఇది అప్పుడప్పుడు వక్రీకృతమైన ఘన స్వరూపంలో కనబడినా తక్కువ తాపోగ్రతల వద్ద వజ్రపు విన్యాసంలోకి మారడం వల్ల వజ్రం వలె పెళుసుగా ఉండి తక్కువ వాహకత్వం ప్రదర్శిస్తుంది.
ఇంతకీ చెప్పొచ్చేదేమిటంటే లోహాలని వర్గీకరణ పేరుతో ఏదో ఒక విధంగా లొంగదీసుకుందామంటే లొంగడం లేదు.
ఆధారాలు
- J. Crowther, “What is a metal?,” Science News, 28, Penguin Books, 1953.
- https://en.wikipedia.org/wiki/Properties_of_metals,_metalloids_and_nonmetals.
- https://www.angelo.edu/faculty/kboudrea/periodic/physical_metals.htm.
- Google Images.

